Den utbredte bruken av små husholdningsapparater blant forbrukere medfører behov for strømkilder, eller enkeltstrømkretser galvaniske celler, ofte kjent som batterier. De dukket først opp i 1800, takket være den italienske fysikeren Alessandro Volta. De varierer i størrelse og form, spenning, kapasitet og batteritype. Alkaliske og saltvannsbatterier er mye brukt i markedet for små apparater og elektronikk.
Hva er saltvannsbatterier?
Saltbatterier — kilder til elektrisk strøm generert i en enkel enhet gjennom en kjemisk reaksjon. De kalles noen ganger karbon-sink-batterier eller karbonbatterier. Denne typen celle regnes som den billigste, men har lav energitetthet, noe som gjør den godt egnet for enheter med lavt strømforbruk. I enheter med høyt strømforbruk eller med karakteristiske økninger i laststrøm og temperatur, varer de ikke lenge og brukes derfor ikke.
Betegnelse av saltbatterier
Betegnelsen på saltbatterier aksepteres i henhold til flere standarder:
- Amerikansk klassifiseringssystem.
- Det internasjonale systemet (IEC).
- Interstatlig standard (GOST).
| Amerikansk klassifiseringssystem | Internasjonal klassifisering IEC | GOST | Størrelse, mm | Kapasitet, mAh |
| EN | R23 | 17x50 | ||
| AA | R6 | 316 | 14,5x50,5 | 1100 |
| AAA | R03 | 286 | 10,5x44,5 | 540 |
| C | R14 | 343 | 26,2x50 | 3800 |
| D | R20 | 373 | 34,2x61,5 | 8000 |
| F | 25 kr | 33x91 | ||
| 1/2AA | 14250 kr | 312 | 14,5x25 | 250 |
| R10 | R10 | 332 | 21,5x37,3 | 1800 |
For eksempel betyr merkingen av et saltvannsbatteri R 6: rund, sylindrisk, finger, salttypeelement, totalmål 14,5x50,5, kapasitet1100 mAh. Standardspenningen er 1,5 V. «R»-betegnelsen (salt) på batterietiketten skiller saltbatterier fra andre typer batterier (alkaliske eller litium).
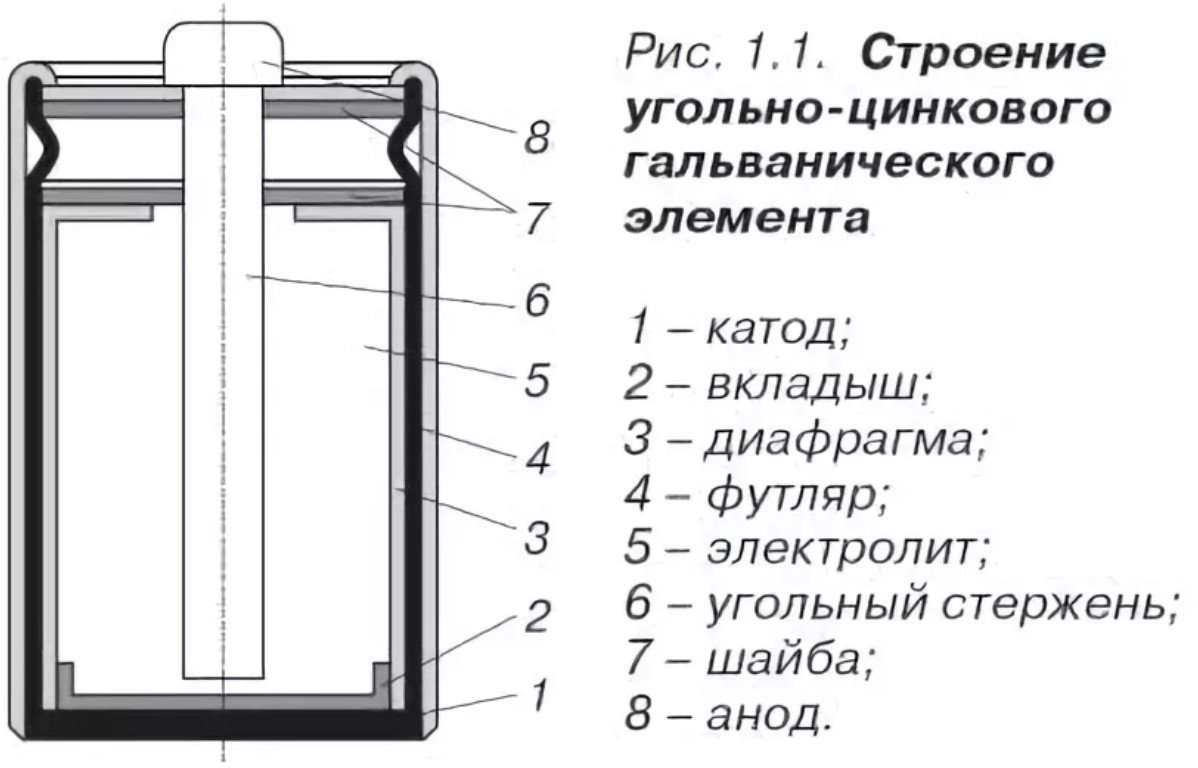
Design og komposisjon
Utformingen av et saltbatteri er ganske enkel og består av:
- Katode - den samme Saltbatteriets deksel er laget laget av sink, med forbedrede korrosjonsbestandige egenskaper og høy renhetsgrad (minus).
- Anoden er et agglomerat, fremstilt ved pressing, impregnert med elektrolytt (pluss).
- Elektrolytt: ammoniumklorid eller sinkklorid, med tilsetning av et fortykningsmiddel (stivelse).
- Karbonstrømleder - går gjennom sentrum, behandlet med parafinblanding.
- Gasskammer - plassert øverst, designet for å samle gasser fra den kjemiske reaksjonen.
- Pakning - plassert øverst, fungerer som tetningsmiddel.
- Beskyttelsesetui - papp eller blikk for å beskytte mot korrosjon og elektrolyttlekkasjer.
La oss se på sammensetningen av et saltbatteri fra et kjemisk synspunkt:
- Katoden er høyrenset sink, motstandsdyktig mot korrosjon.
- Anode - MnO-blanding2, grafitt, elektrolyttimpregnering.
- Elektrolytten er ammoniumklorid, eller en blanding av sinkklorid og kalsiumklorid.
Hvilke batterier er bedre: saltvann (1) eller alkaliske (2)?
Sammenligningen kan gjøres i form av en tabell, hvor fordeler og ulemper ved ulike typer elementer er tydelig synlige:
| Sammenligningsparametere | 1 | 2 |
| Temperaturforhold, driftsforhold | Ytelsen reduseres ved lave temperaturer og tåler ikke strømstøt. | Fungerer bra ved lave temperaturer - ned til -20Å, tåler lett overspenninger, er ikke redde for en kraftig økning i laststrømmen |
| Best før-dato | 2–3 år | 5 år |
| Søknad | Egnet for bruk i enheter med lavt strømforbruk | Egnet for bruk i utstyr med middels og høyt energiforbruk |
| Instrumenter, tekniske apparater | Vekkerklokker, veggklokker, fjernkontroller, mini-lommelykter, enkle leker | Spillere, lommelykter, musikalske leker, stemmeopptakere, blodtrykksmålere |
Når du velger en strømkilde for en enhet med spesifikke driftskrav, er det viktig å vite hvordan man skiller mellom et saltvannsbatteri og et alkalisk batteri. Saltvannsbatterier er merket med bokstaven R, mens alkaliske batterier er innledet med bokstaven L (LR).
Konklusjoner og anbefalinger
Denne typen strømkilde er lettere og rimeligere. Saltvannsbatterier har imidlertid kort holdbarhet – 2 til 3 år – og de kan delvis selvutlades under lagring og under bruk ved en plutselig strømstøt. Gitt deres relativt dårlige ytelse, men relativt lave kostnad, er det derfor enkelt å kjøpe flere sett med batterier som en backup.
Ikke høy kapasitetsaltbatterier (2–3 ganger mindre enn andre typer) begrenser bruken til enkle enheter med lav laststrøm.
Det er enkelt å avgjøre om det er mulig å lade saltvannsbatterier: batteriets navn er angitt på enheten som er beregnet for lading. kapasitetI mAh. Hvis denne verdien ikke er tilgjengelig, er det et vanlig batteri, og til tross for en rekke ekspertråd, bør du ikke lade det. Lading vil ikke gi den forventede langsiktige effekten og kan føre til en ulykke på grunn av overoppheting og elektrolyttlekkasje. Hvis du trenger en mer pålitelig og langvarig strømkilde, er det bedre å investere i et alkalisk alternativ eller et oppladbart batteri.
Interessant faktum: Gjør-det-selv saltbatteri Det kan lages veldig enkelt. Du trenger 50-kopek-mynter, folie, papir og en saltløsning. Det er best å bløtlegge myntene i en eddikløsning før bruk for å fjerne plakk eller smuss. Monter enheten: en mynt, papir dynket i saltløsningen og folie. Gjenta denne prosessen flere ganger, og lag en søyle med mynten (positiv) i den ene enden og folien (negativ) i den andre. Strøm genereres av potensialforskjellen som skapes av elektrolytten (saltløsningen) mellom metallet i folien og mynten. Denne oppfinnelsen kalles en voltaisk haug, og spenningen avhenger direkte av antall mynter som brukes: jo flere mynter det er, desto høyere spenning oppnås. Etter eksperimentet er imidlertid myntene ikke lenger brukbare; de vil ha et rustent belegg.